2024 年 4 月5日,美国食品药品监督管理局(FDA) 批准了ciltacabtagene autoleucel (西达基奥仑赛) 用于治疗既往接受过一种或多种治疗的难治性或复发性多发性骨髓瘤。这种治疗可用于对来那度胺无反应且先前接受过免疫调节剂和蛋白酶体抑制剂的患者。
美国食品药品监督管理局(FDA)根据3期临床试验CARTITUDE-4的结果批准了该治疗。该临床试验的结果已在2023年美国临床肿瘤学会 (ASCO) 年会上公布。结果显示:西达基奥仑赛组的无进展生存率为75.9%,标准治疗组为48.6%;西达基奥仑赛组比标准治疗组有更多的患者完全缓解或更好(73.1% vs 21.8%),总体缓解(部分缓解或更好)分别为84.6%和67.3%,在有反应的患者中,西达基奥仑赛组估计有84.7%的患者持续至少12个月有反应,而标准治疗组为63.0%。

西达基奥仑赛是传奇生物自主研发的一款具有两种靶向B细胞成熟抗原(BCMA)单域抗体的嵌合抗原受体(CAR)T细胞免疫疗法。
2022年2月,美国FDA正式批准西达基奥仑赛上市,用于治疗复发/难治性多发性骨髓瘤(R/R MM)患者。这是全球第二款获FDA批准的BCMA CAR-T,也是首款获FDA批准的国产CAR-T细胞疗法。

根据2023年欧洲血液学协会(EHA)大会上公布的1b/2期CARTITUDE-1研究(NCT03548207)的最终结果显示:总缓解率(ORR)高达97.9%,其中包括82.5%的严格完全缓解(CR)患者。此外,12.4%的患者有非常好的部分缓解,3.1%的患者经历了部分缓解(PR)。中位无进展生存期(PFS)为34.9个月,中位缓解持续时间(DOR)为33.9个月。
多发性骨髓瘤(Multiple myeloma, MM)是一种浆细胞恶性肿瘤,约占血液系统恶性肿瘤的10%。据统计,我国多发性骨髓瘤每年新发病例数高达27800例,作为一种多发于老年人的恶性血液肿瘤,随着我国人口老龄化的加速,多发性骨髓瘤的发病率也将逐年上升。多发性骨髓瘤目前仍无法治愈,多数多发性骨髓瘤患者会出现骨头疼痛、骨折,约半数患者会出现肾脏损伤,甚至需要进行血液透析,严重影响患者生存。被称为“吃骨头”的血液病。
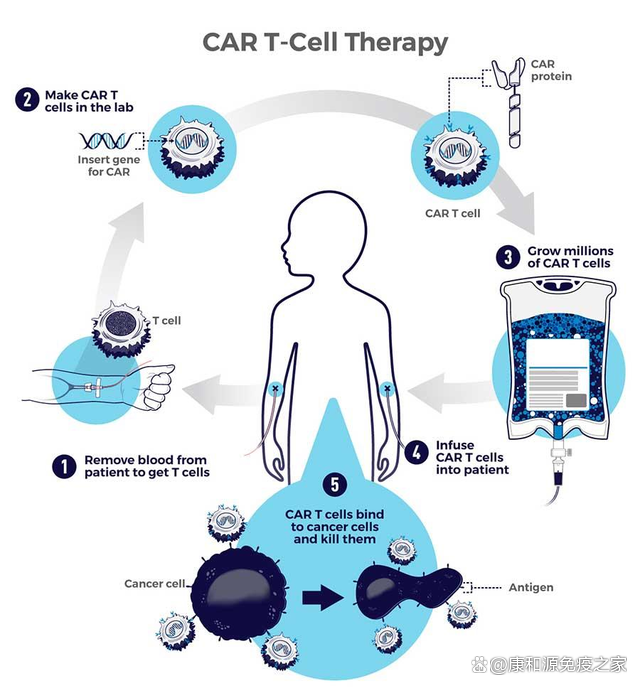
近年来热门的CAR-T细胞疗法,就是将病人自身免疫系统的T细胞提取出来,经过体外培养和改造,给这些T细胞装备上特殊分子,使它们能识别并攻击特定的靶细胞,再把改造过后的T细胞注射回病人身体,由这些T细胞来消灭靶细胞。
自体CAR-T产品:泽沃基奥仑赛
3月1日,国家药品监督管理局正式下达通知,批准泽沃基奥仑赛注射液用于治疗复发或难治性多发性骨髓瘤成人患者,既往经过至少3线治疗后进展(至少使用过一种蛋白酶体抑制剂及免疫调节剂)。
泽沃基奥仑赛是一种针对BCMA的自体CAR-T产品,具有全人源 BCMA 特异性单链可变片段的CAR构建体,旨在具有更低的免疫原性和更高的稳定性。
此次获批是基于一项在中国进行的开放标签、单臂、多中心II期的临床试验(LUMMICAR STUDY 1,NCT03975907)。根据2022年美国血液学会(“ASH”)公布的试验结果,泽沃基奥仑赛表现出令人鼓舞的疗效和良好的安全性。从2019年7月23日开始,14名中位年龄为54岁(范围34,62岁)的患者接受了单次泽沃基奥仑赛输注。截至数据截止日期(2023年7月17日),中位生存随访时间为37.7个月。总缓解率为100%,其中11例(78.6%)患者达到完全缓解(CR)或严格完全缓解(sCR),2例(14.3%)患者获得了很好的部分缓解,1例(7.1%)患者获得了部分缓解。所有达到CR或CR以上的患者微小残留病灶(MRD)均为阴性。所有患者的中位无进展生存期为25.0个月,sCR/CR患者的中位无进展生存期为26.9个月。

所有患者的中位缓解持续时间为24.1个月,sCR/CR患者的中位缓解持续时间为26.0个月。在数据截止时,5名受试者仍有持续的反应。

众所周知CAR-T生产成本高,很难降价。但是这事被印度人做到了。
二三十万的CAR-T产品—NexCAR19,缓解率达70%!
3月21日,《自然》期刊发布印度研发出一种经济实惠的CAR-T细胞疗法—NexCAR19,已获中央药品标准控制组织(CDSCO)批准震撼上市,用于治疗血液癌症。该疗法单次治疗费用在3万~4万美元(约20万~30万人民币)。

据了解,NexCAR19在患有不同形式淋巴瘤和白血病的成人中的早期临床试验表明,在接受治疗的33人中,有19人在一个月的随访中肿瘤完全消失。另外四个人的肿瘤缩小了一半,总体缓解率为70%。2023年12月在美国血液学会会议上公布的试验结果显示,两项试验中 67% 的患者(53人中有36人)的癌症程度显著下降(客观反应),大约一半的肿瘤完全消失(完全缓解)。
这无疑是一项重大的突破,大大降低了患者的经济负担,虽然对于普通民众而言,NexCAR19的价格仍然不菲,但相较于百万“天价”的CAR-T产品无疑是一项重大的突破!国内CAR-T价格高,多数是因为原材料、耗材、设备等离不开进口,生产成本高。但是国内的CAR-T技术也在持续研究发展中,相信在多方努力下,这一疗法能有更多降价的好消息传来。
相信未来更多企业通过探索掌握这项技术后,价格也会降下来,惠及大多数患者。
免责声明:康和源免疫之家为免疫科普平台,文本参考来源于网络,版权归原作者所有。
该文章仅供分享,如涉嫌侵犯您的著作权请联系我们删除,谢谢!
参考资料
Cutting-edge CAR-T cancer therapy is now made in India — at one-tenth the cost (nature.com)
